Study on the relationship between anti-inflammatory cytokine IL-35 and delayed renal graft function
-
摘要:目的 探讨白细胞介素(IL)-35与移植肾功能恢复情况之间的关系。方法 回顾性分析45例心脏死亡器官捐献(DCD)供肾肾移植受体的临床资料。根据肾移植术后是否发生移植物功能延迟恢复(DGF),所有受体分为早期肾功能恢复良好(IGF)组(32例)和DGF组(13例)。比较肾移植术后1、2、3、7、14、28 d及术后3个月、6个月、1年各时间点两组受体的血清肌酐(Scr)和估算肾小球滤过率(eGFR)水平;比较肾移植术后1、2、3、7、14、28 d各时间点两组受体血清和尿液IL-35含量。结果 DGF组受体术后肾功能恢复迟缓,术后7 d时Scr水平高于IGF组,eGFR水平低于IGF组,差异均有统计学意义(均为P < 0.05)。术后1年,两组受体Scr水平的差异无统计学意义,但eGFR仍存在较大差异,与IGF组相比,DGF组受体术后1年时eGFR仍降低(P < 0.05)。术后1、2、3、7、14 d,DGF组血清中IL-35含量均低于IGF组,两组比较差异均有统计学意义(均为P < 0.05);术后28 d,与IGF组相比,DGF组血清IL-35含量反而升高,两组比较差异有统计学意义(P < 0.05)。术后1、2、3、7 d,DGF组尿液中IL-35含量均低于IGF组,两组比较差异均有统计学意义(均为P < 0.05);术后14、28 d,两组受体尿液IL-35含量进行比较,差异均无统计学意义(均为P > 0.05)。结论 肾移植术后受体血清和尿液中IL-35含量低与DGF发生存在一定的联系,提示术后早期受体全身和移植肾局部抑炎应答过弱,过度的炎症应答得不到有效控制,可能是DGF发生的重要原因。
-
关键词:
- 肾移植 /
- 抑炎细胞因子 /
- 白细胞介素-35(IL-35) /
- 移植物功能延迟恢复(DGF) /
- 炎症应答 /
- 缺血-再灌注损伤(IRI) /
- 血清肌酐(Scr) /
- 估算肾小球滤过率(eGFR)
Abstract:Objective To investigate the relationship between the interleukin (IL)-35 and the recovery of renal graft function.Methods Clinical data of 45 recipients receiving renal transplantation from donation after cardiac death (DCD) were retrospectively analyzed. According to the presence of delayed graft function (DGF) after renal transplantation, all recipients were divided into the immediate graft function (IGF) group (n=32) and DGF group (n=13). The serum creatinine (Scr) level and estimated glomerular filtration rate (eGFR) in the recipients were statistically compared between two groups at 1, 2, 3, 7, 14, 28 d and 3, 6 and 12 months after renal transplantation. The IL-35 levels in the serum and urine samples of the recipients were statistically compared between two groups at 1, 2, 3, 7, 14, 28 d following renal transplantation.Results In the DGF group, the renal function was restored slowly. Compared with the IGF group, the Scr level was significantly higher, whereas the eGFR was considerably lower in the DGF group at postoperative 7 d (both P < 0.05). At 1 year after surgery, there was no significant difference in the Scr level between two groups. Compared with the IGF group, the eGFR in the DGF group was significantly lower at postoperative 1 year (P < 0.05). At 1, 2, 3, 7, 14 d after operation, the serum levels of IL-35 in the DGF group were evidently lower than those in the IGF group (all P < 0.05). Compared with the IGF group, the serum level of IL-35 in the DGF group was significantly increased at postoperative 28 d (P < 0.05). At postoperative 1, 2, 3, 7 d, the IL-35 levels in the urine samples in the DGF group were significantly lower than those in the IGF group (all P < 0.05). At postoperative 14 and 28 d, the IL-35 levels in the urine samples did not significantly differ between two groups (both P > 0.05).Conclusions The low levels of IL-35 in the serum and urine of recipients after renal transplantation are associated with the incidence of DGF to certain extent, prompting that excessively weak systemic and local anti-inflammatory responses early after renal transplantation and uncontrolled excessive inflammatory response are probably the pivotal causes of DGF. -
移植物功能延迟恢复(DGF)是肾移植术后较为常见的并发症[1],接受不同类型供肾的受体术后DGF发生率存在较大差异,接受亲属活体供肾的受体术后DGF发生率约3.4%,而接受心脏死亡器官捐献(DCD)供肾的受体术后DGF发生率高达37.1%[2]。肾移植过程中,缺血-再灌注损伤(IRI)引起的急性肾小管坏死是DGF发生的主要原因[3]。肾IRI时,肾小管上皮细胞趋化因子和促炎因子[例如肿瘤坏死因子(TNF)-α、白细胞介素(IL)-1β、IL-6等]表达上调,进一步募集和活化单核巨噬细胞、中性粒细胞至移植肾局部,加重肾损伤[4]。另一方面,肾小管上皮细胞也能分泌抑炎因子[例如转化生长因子(TGF)-β、IL-10等],发挥限制炎症应答的作用,避免炎症应答对移植肾的过度损伤[5]。因此,IRI过程中,抑炎应答在保护移植肾功能,避免过度的炎症应答所致移植肾损伤中发挥重要作用。IL-35是新发现的具有免疫抑制功能的细胞因子[6],在各类炎症疾病中发挥重要抗炎作用[7],IL-35在肾IRI中的作用笔者尚未见报道。因此,本研究通过动态监测肾移植术后受体血清和尿液中IL-35含量,分析其与DGF之间的关系,以探讨IL-35含量变化在肾IRI所致DGF中的作用。
1. 资料与方法
1.1 研究对象
回顾性分析2015年9月至2017年3月于苏州大学附属第一医院接受DCD供肾移植受体临床资料,排除样本收集缺失、临床资料不完整者,最终纳入研究病例45例,其中男31例,女14例,平均年龄37岁。所有受体群体反应性抗体均为阴性,补体依赖淋巴细胞毒性试验(CDC)1.2%~5.8%。原发病分别为慢性肾小球肾炎28例,糖尿病肾病10例,多囊肾3例,其他4例。术前血液透析30例,腹膜透析12例,尚未透析3例。所有患者均签署知情同意书,经医院医学伦理委员会批准。
1.2 分组与标准
本研究参照美国器官资源共享网络(UNOS),将DGF定义为肾移植术后出现少尿或无尿,术后7 d内至少需要透析治疗1次[1]。根据肾移植术后是否发生DGF,受体分为早期肾功能恢复良好(immediate graft function,IGF)组[32例,术后7 d内血清肌酐(Scr)恢复至135 µmol/L以下或内生肌酐清除率升高至40 mL/min以上]和DGF组(13例,术后7 d内因少尿或无尿至少需要透析治疗1次)。IGF组,男21例,女11例,年龄(38±8)岁,热缺血时间(9.0±2.2)min,冷缺血时间(16.4±5.3)h;DGF组,男10例,女3例,年龄(38±9)岁,热缺血时间(8.0±2.5)min,冷缺血时间(19.0±4.5)h。两组受体在年龄、性别、免疫抑制方案、透析方式、热缺血时间、冷缺血时间以及人类白细胞抗原(HLA)错配等方面,差异均无统计学意义(均为P > 0.05)。两组受体均排除急性排斥反应、感染、泌尿道梗阻等并发症。
1.3 免疫抑制方案及DGF治疗方案
免疫抑制方案:所有受体术前均采用免疫诱导治疗,37例采用抗人T细胞免疫球蛋白(ALG)100 mg/d,连用3~5 d;8例采用巴利昔单抗(舒莱)20 mg/d,术前和术后第4日各用1次。免疫抑制维持方案采用钙神经蛋白抑制剂(CNI)+吗替麦考酚酯(MMF)+肾上腺皮质激素(激素)三联免疫抑制方案。术中使用甲泼尼龙0.5 g,术后前3日按体质量给予甲泼尼龙6~8 mg/kg,术后第4日开始口服Pred 70 mg/d,每日减少5 mg,至20 mg/d维持,术后1个月降为15 mg/d。
肾移植术后13例受体发生DGF,依据受体情况给予血液透析或腹膜透析、预防排斥反应、头孢哌酮钠舒巴坦钠预防细菌感染、卡泊芬净预防真菌感染、营养支持等治疗,积极监测血常规、肾功能、CNI及MMF血药浓度,等待移植肾功能恢复。其中1例受体术后1周因血管因素严重出血,行移植肾切除(术后7 d后的数据不包括本例受体)。其余12例受体肾功能均恢复良好,顺利出院。
1.4 研究方法
收集受体肾移植术后1、2、3、7、14、28 d及术后3个月、6个月、1年的住院和门诊随访资料,包括生化全套、血清药物浓度、尿常规,使用公式计算不同时间点估算肾小球滤过率(estimated glomerular filtration rate,eGFR)[8],比较各时间点两组受体的Scr和eGFR水平。收集受体肾移植术后1、2、3、7、14、28 d不抗凝外周血样本3~5 mL和晨尿标本50 mL,离心收集血清或上清,分装后标本冻存于-80 ℃。取上述冻存的血清、尿液标本,采用酶联免疫吸附试验(ELISA)试剂盒(中国武汉优尔生有限公司)检测IL-35含量,按照操作说明书进行,比较各时间点两组受体血清和尿液IL-35含量。
1.5 统计学方法
采用SPSS 13.0软件进行统计学分析。临床及实验室计量资料采用均数±标准差表示,两组样本比较采用t检验,P < 0.05为差异有统计学意义。
2. 结果
2.1 DGF组与IGF组受体术后1年内肾功能的比较
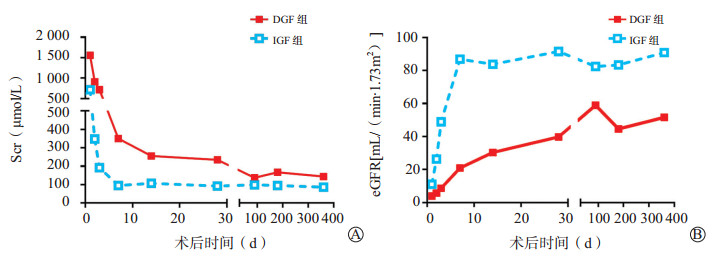
两组受体术后不同时间点Scr和eGFR水平的比较见图 1。DGF组受体术后肾功能恢复迟缓,术后7 d时Scr(350±167)µmol/L,高于IGF组的(95±25)µmol/L,差异有统计学意义(P < 0.05);术后7 d时IGF组eGFR(87±32)mL/(min·1.73 m2),高于DGF组的(21±13)mL/(min·1.73 m2)。随访至术后1年,两组受体Scr水平的差异无统计学意义,但eGFR仍存在较大差异,与IGF组相比,DGF组受体术后1年时eGFR仍降低[(91±41)mL/(min·1.73 m2)比(52±9)mL/(min·1.73 m2),P < 0.05]。
2.2 DGF组与IGF组血清和尿液IL-35含量的比较
通过动态检测肾移植受体术后各时间点受体血清IL-35的含量(图 2A),我们发现术后1 d,DGF组IL-35含量(39±15)pg/mL,低于IGF组的(53±16)pg/mL,两组比较差异有统计学意义(P < 0.05);术后2、3、7 d,DGF组IL-35含量仍低于IGF组,直至术后14 d,DGF组血清IL-35含量仍低于IGF组[(49±17)pg/mL比(58±10)pg/mL,P < 0.05]。术后28 d,与IGF组相比,DGF组血清IL-35含量反而升高,两组比较差异有统计学意义[(50±7)pg/mL比(64±11)pg/mL,P < 0.05]。
通过检测肾移植受体术后各时间点受体尿液IL-35的含量(图 2B),发现术后1 d,DGF组IL-35含量(28±9)pg/mL,低于IGF组的(52±7)pg/mL,两组比较差异有统计学意义(P < 0.05);术后2、3 d,DGF组IL-35含量仍低于IGF组,直至术后7 d,IGF组尿液IL-35含量仍持续低于IGF组[(17±5)pg/mL比(41±7)pg/mL,P < 0.05]。术后14、28 d,两组受体尿液IL-35含量进行比较,差异均无统计学意义(均为P > 0.05)。
3. 讨论
DGF是肾移植过程中出现的急性肾损伤(acute kidney injury,AKI)的表现形式,是肾移植术后较为常见的并发症[1]。DGF不仅影响移植肾早期功能的恢复,而且增加急性排斥反应的风险[9]。尽管目前对DGF是否影响移植肾的长期存活尚存在争议,但Yarlagadda等[1]通过对39 635例肾移植受体资料分析发现,DGF使受体术后第1年急性排斥反应风险增加38%,移植物失功风险增加41%;随访至3.5年,与IGF组比较,DGF组Scr水平明显升高。本研究45例肾移植受体中,DGF发生率相对较高,为28.9%,可能与本组研究对象均来源于DCD供肾有关,该结果与国内陈国栋等[10]报道基本一致,他们通过分析DCD肾移植特征,发现DGF发生率为29%。本研究对术后1年内两组受体Scr和eGFR水平进行比较,发现尽管半年后两组受体Scr水平无明显差异,但DGF组受体术后1年时eGFR仍相对较低,提示DGF不仅影响移植肾早期功能恢复,也会影响移植肾功能的长期恢复。
肾IRI驱动的炎症应答在DGF发生、发展和预后中发挥着重要作用[11]。炎症应答不仅在机体清除坏死细胞中发挥重要作用,而且在组织损伤和修复中的作用也不可或缺[12]。肾IRI炎症过程始于血管内皮细胞和肾小管上皮的缺血缺氧性损伤,坏死的细胞释放一系列炎症因子[如IL-1β、IL-6、TNF-α、单核细胞趋化蛋白(monocyte chemotactic protein,MCP)-1],进入肾组织和血液循环[13],进一步募集中性粒细胞、单核巨噬细胞和淋巴细胞至移植肾局部,发生炎症应答,参与移植肾的损伤和修复[14]。促炎和抑炎应答的平衡与否,决定了组织损伤和修复的程度,最终影响移植肾的预后[15]。本研究中45例肾移植受体的供肾均来源于DCD供体,肾IRI均不可避免,但13例发生DGF,而32例受体肾功能恢复良好。临床实践中,我们发现来源于同一供体的2例受体,尽管供肾情况完全一致,冷缺血时间也相同,然而,1例受体术后发生DGF,另1例受体移植肾功能恢复良好,推测其主要原因与IRI所致受体全身及肾脏局部炎症应答强度不同相关。Guerrieri等[11]通过检测肾移植术后7 d移植肾穿刺标本中炎症基因的表达情况,发现促炎因子IFN-γ、IL-1β、血红素加氧酶(HO)-1表达水平升高,且与DGF呈正相关,而抑炎因子TGF-β表达降低,与DGF呈负相关,提示DGF的发生与促炎因子和抑炎因子间表达失衡相关。因此,我们重点关注具有抑炎功能的细胞因子IL-35,探索其在肾移植术后移植肾功能恢复中的作用。
IL-35是新近发现的具有免疫抑制功能的分泌型细胞因子,主要由调节性T细胞分泌,主要功能是诱导辅助性T细胞(helper T cell,Th)1细胞产生,抑制Th17细胞分化和IL-17的产生[16]。IL-35与炎症性疾病关系密切,在类风湿性关节炎中,IL-35含量高能减轻关节炎症[17];多发性硬化患者中,循环中IL-35含量高低与疾病程度相关,并且与治疗的效果相关[18];病毒性心肌炎中,促进IL-35表达能够通过抑制Th17型免疫应答,减轻心肌炎严重程度,提高存活率[19]。最新研究发现,IL-35过表达能够降低Th1型细胞免疫应答,促进分泌IL-10的T细胞增殖,降低骨髓移植中移植物抗宿主病(GVHD)的发生[20]。上述研究均提示IL-35具有免疫抑制作用,在炎症性疾病中发挥重要免疫调节作用,是机体重要的内源性免疫抑制蛋白。本研究中,我们动态监测IL-35含量在移植肾功能延迟恢复者(DGF组)和早期肾功能恢复良好者(IGF组)血清、尿液中的变化,发现肾移植术后1、2 d,两组受体血清和尿液IL-35含量均呈现快速上升,而后迅速下降,但DGF组血清和尿液IL-35含量在术后1周内始终低于IGF组,提示肾移植术后早期IRI所致受体全身和移植肾局部抑炎应答过弱,过度的炎症应答得不到有效控制,可能是导致DGF的重要原因。因此,肾移植术后早期,炎症应答自稳态被打破,以IL-35为代表的抑炎因子低水平表达,导致IRI过程中抑炎应答过弱,可能是DGF发生的危险因素。
综上所述,肾移植受体术后DGF组血清和尿液IL-35含量较低,与IGF组存在明显差异,提示IL-35在移植肾IRI的致病机制中可能发挥了一定的作用,是限制过度炎症应答肾损伤的重要因素。本研究的临床意义在于,通过检测血清、尿液IL-35含量的变化情况,有助于判断术后早期受体炎症应答强度和移植肾损伤程度,及时采取有效治疗措施进行干预,减少移植肾的炎症损伤,最大限度地减少DGF的发生。但目前IL-35在肾IRI中的确切作用机制及与肾IRI修复间的关系尚不明确,仍需要进一步研究证实。
-
-
[1] YARLAGADDA SG, COCA SG, FORMICA RN JR, et al. Association between delayed graft function and allograft and patient survival: a systematic review and Meta-analysis[J]. Nephrol Dial Transplant, 2009, 24(3): 1039-1047. DOI: 10.1093/ndt/gfn667.
[2] COLLINS AJ, FOLEY RN, HERZOG C, et al. US Renal Data System 2010 Annual Data Report[J]. Am J Kidney Dis, 2011, 57(1 Suppl 1): A8, e1-e526. DOI: 10.1053/j.ajkd.2010.10.007.
[3] SIEDLECKI A, IRISH W, BRENNAN DC. Delayed graft function in the kidney transplant[J]. Am J Transplant, 2011, 11(11): 2279-2296. DOI: 10.1111/j.1600-6143.2011.03754.x.
[4] LINFERT D, CHOWDHRY T, RABB H. Lymphocytes and ischemia-reperfusion injury[J]. Transplant Rev (Orlando), 2009, 23(1): 1-10. DOI: 10.1016/j.trre.2008.08.003.
[5] KINSEY GR, SHARMA R, HUANG L, et al. Regulatory T cells suppress innate immunity in kidney ischemia-reperfusion injury[J]. J Am Soc Nephrol, 2009, 20(8): 1744-1753. DOI: 10.1681/ASN.2008111160.
[6] COLLISON LW, WORKMAN CJ, KUO TT, et al. The inhibitory cytokine IL-35 contributes to regulatory T-cell function[J]. Nature, 2007, 450(7169): 566-569. DOI: 10.1038/nature06306
[7] WU S, LI Y, LI Y, et al. Interleukin-35 attenuates collagen-induced arthritis through suppression of vascular endothelial growth factor and its receptors[J]. Int Immunopharmacol, 2016, 34:71-77. DOI: 10.1016/j.intimp.2016.02.018.
[8] MA YC, ZUO L, CHEN JH, et al. Modified glomerular filtration rate estimating equation for Chinese patients with chronic kidney disease[J]. J Am Soc Nephrol, 2006, 17(10): 2937-2944. DOI: 10.1681/ASN.2006040368
[9] GROSSO G, CORONA D, MISTRETTA A, et al. Delayed graft function and long-term outcome in kidney transplantation[J]. Transplant Proc, 2012, 44(7): 1879-1883. DOI: 10.1016/j.transproceed.2012.06.044.
[10] 陈国栋, 袁小鹏, 李军, 等.心脏死亡器官捐献供肾与传统尸体供肾肾移植的疗效比较[J].中华器官移植杂志, 2013, 34(7): 392-395. DOI: 10.3760/cma.j.issn.0254-1785.2013.07.003.CHEN CHEN GD, YUAN XP, LI J, et al. Comparison of long-term efficacy and complications after kidney transplantation between donors after cardiac death and traditional deceased donors[J]. Chin J Organ Transplant, 2013, 34(7): 392-395. DOI: 10.3760/cma.j.issn.0254-1785.2013.07.003.
[11] GUERRIERI D, RE L, PETRONI J, et al. Gene expression profile in delay graft function: inflammatory markers are associated with recipient and donor risk factors[J]. Mediators Inflamm, 2014: 167361. DOI: 10.1155/2014/167361.
[12] PATSCHAN D, PATSCHAN S, MÜLLER GA. Inflammation and microvasculopathy in renal ischemia reperfusion injury[J]. J Transplant, 2012: 764154. DOI: 10.1155/2012/764154.
[13] KIELAR ML, JOHN R, BENNETT M, et al. Maladaptive role of IL-6 in ischemic acute renal failure[J]. J Am Soc Nephrol, 2005, 16(11): 3315-3325. DOI: 10.1681/ASN.2003090757
[14] ASCON M, ASCON DB, LIU M, et al. Renal ischemia-reperfusion leads to long term infiltration of activated and effector-memory T lymphocytes[J]. Kidney Int, 2009, 75(5): 526-535. DOI: 10.1038/ki.2008.602.
[15] RABB H, GRIFFIN MD, MCKAY DB, et al. Inflammation in AKI: current understanding, key questions, and knowledge gaps[J]. J Am Soc Nephrol, 2016, 27(2): 371-379. DOI: 10.1681/ASN.2015030261.
[16] NIEDBALA W, WEI XQ, CAI B, et al. IL-35 is a novel cytokine with therapeutic effects against collagen-induced arthritis through the expansion of regulatory T cells and suppression of Th17 cells[J]. Eur J Immunol, 2007, 37(11): 3021-3029. DOI: 10.1002/(ISSN)1521-4141
[17] THIOLAT A, DENYS A, PETIT M, et al. Interleukin-35 gene therapy exacerbates experimental rheumatoid arthritis in mice[J]. Cytokine, 2014, 69(1): 87-93. DOI: 10.1016/j.cyto.2014.05.015.
[18] JAFARZADEH A, JAMALI M, MAHDAVI R, et al. Circulating levels of interleukin-35 in patients with multiple sclerosis: evaluation of the influences of FOXP3 gene polymorphism and treatment program[J]. J Mol Neurosci, 2015, 55(4): 891-897. DOI: 10.1007/s12031-014-0443-z.
[19] HU Y, DONG C, YUE Y, et al. In vivo delivery of interleukin-35 relieves coxsackievirus-B3-induced viral myocarditis by inhibiting Th17 cells[J]. Arch Virol, 2014, 159(9): 2411-2419. DOI: 10.1007/s00705-014-2098-z.
[20] LIU Y, WU Y, WANG Y, et al. IL-35 mitigates murine acute graft-versus-host disease with retention of graft-versus-leukemia effects[J]. Leukemia, 2015, 29(4): 939-946. DOI: 10.1038/leu.2014.310.
-
期刊类型引用(4)
1. 梁丽薇,赵晶凤,李亚静,甘雨. 百令胶囊联合厄贝沙坦治疗CGN的疗效研究. 重庆医学. 2021(04): 595-598 .  百度学术
百度学术
2. 刘洪,刘东亮,周果,陈琴,彭志飞,文婧妤,钟山,王筱啸,狄文佳,熊玮,冉清,杨洪吉. CEUS对早期移植肾功能延迟恢复预测价值的临床研究. 实用器官移植电子杂志. 2021(05): 364-371 .  百度学术
百度学术
3. 刘幸,李海雯,黄红丽,沈凌筠,张乐,刘向芳,张文林,王璐. 益生菌强化肠内营养支持对重症急性胰腺炎患者胃肠道功能和炎症因子的影响. 昆明医科大学学报. 2021(11): 81-86 .  百度学术
百度学术
4. 樊雪梅,容松. 蛋白激酶Cβ抑制剂对肾缺血-再灌注损伤模型及其巨噬细胞亚型表达的影响. 器官移植. 2019(04): 423-428 .  本站查看
本站查看
其他类型引用(1)



 下载:
下载:



