Breeding and identification of Wuzhishan miniature pigs with α-1, 3 galactosyltransferase gene-knockout
-
摘要:目的 总结α-1,3半乳糖基转移酶(GGTA1)基因敲除(GTKO)五指山小型猪的繁育和鉴定。方法 统计GTKO五指山小型猪的繁育结果及窝产仔数;采用PCR技术对GTKO五指山小型猪GGTA1基因敲除类型进行鉴定;采用荧光显微镜和流式细胞术对人、野生型五指山小型猪、GTKO五指山小型猪外周血单核细胞(PBMC)的αGal表型进行检测;比较GTKO五指山小型猪与野生型五指山小型猪血常规指标的差异。结果 GGTA1基因型的遗传符合孟德尔定律;GGTA1-/-猪的PBMC流式检测无荧光表达,与基因型鉴定结果一致;GTKO五指山小型猪雌性猪初产窝产仔数为(6.8±1.8)只,经产窝产仔数为(8.3±2.2)只;血常规检测的各项指标与野生型五指山小型猪差异均无统计学意义(均为P>0.05)。结论 连续2代GTKO五指山小型猪遗传稳定,繁殖力正常。GTKO五指山小型猪可作为异种器官移植研究的可靠供体。
-
关键词:
- 琢-1, 3-半乳糖基转移酶 /
- 基因敲除 /
- 五指山小型猪 /
- 繁殖性能 /
- 琢-1, 3-半乳糖表型 /
- 外周血单
Abstract:Objective To summarize the breeding and identification of Wuzhishan miniature pig models with α-1, 3 galactosyltransferase (GGTA1) gene-knockout (GTKO).Methods The breeding and reproduction perform of GTKO Wuzhishan miniature pigs were assessed and the quantity of piglets was counted. The GTKO Wuzhishan miniature pig models with GGTA1gene knockout were validated by polymerase chain reaction (PCR). The αGal phenotype of peripheral blood mononuclear cells (PBMC) in human, wild-type Wuzhishan miniature pigs and GTKO Wuzhishan miniature pigs was detected by fluorescent microscope and flow cytometry. Routine blood test parameters were statistically compared between the GTKO and wild-type Wuzhishan miniature pigs.Results The inheritance of GGTA1 genotype complied with Mendel's law. Flow cytometry detected no fluorescent expression of PBMC in GGTA1-/- pig models, which were consistent with the genotype identification results. The mean piglets of the primiparous GTKO Wuzhishan miniature pigs were (6.8±1.8) and (8.3±2.2) for the multiparous Wuzhishan miniature pigs. No statistical significance was noted in routine blood test parameters between the GTKO and wild-type Wuzhishan miniature pigs (all P>0.05).Conclusions Stable inheritance and normal reproductive capacity are observed in two generations of Wuzhishan miniature pigs continuously. GTKO Wuzhishan miniature pig is a reliable donor for heterogeneous organ transplantation. -
供体器官的严重短缺使许多患者因等不到所需的器官而死亡,成为亟待解决的社会问题,解决这一问题的重要途径是利用基因修饰猪的器官作为供体进行异种移植。猪有望成为异种器官移植的理想供体[1-2],猪的器官移植到人体会发生多种免疫排斥反应,首先是超急性排斥反应(hyperacute rejection,HAR),移植器官与受体血管接通数分钟至24 h内发生排斥反应而丧失功能。导致HAR的主要原因是受体体内天然抗体识别猪细胞表面的α-1, 3-半乳糖(αGal),αGal是由α-1, 3半乳糖基转移酶(α-1, 3-galactosyltransferase,GGTA1)催化合成的[3]。猪GGTA1基因敲除可去除αGal抗原,解决HAR[4]。本实验室于2010年建立了同源重组技术敲除GGTA1基因和体细胞克隆获得单等位基因敲除小型猪技术[5];2012年建立了类转录激活因子效应物核酸酶(transcription activator-like effector nuclease,TALEN)技术敲除GGTA1基因和利用体细胞克隆获得双等位基因敲除小型猪[6]。通过基因敲除和体细胞克隆技术获得了3只健康并能正常繁育的GGTA1基因敲除(GTKO)五指山小型猪,由3只GTKO五指山小型猪繁育建立了GTKO五指山小型猪家系。国外对GTKO大白猪的繁育进行了研究[7],本研究对GTKO五指山小型猪的遗传和繁育进行探讨,为GTKO猪的繁育和进一步多基因修饰奠定基础。
1. 材料与方法
1.1 实验动物
GTKO五指山小型猪和野生型五指山小型猪均饲养在北京安定猪选育有限公司普通级猪舍,自由采食。
1.2 主要试剂与仪器
Premix LA Taq DNA聚合酶、ZR Genomic DNATM-Tissue MiniPrep试剂盒、BD Pharm LyseTM、异硫氰酸荧光素(FITC)标记的植物凝集素(FITC-BS-I-B4)、杜氏磷酸盐缓冲液(Dulbecco's phosphate-buffered saline,DPBS)。倒置显微镜(Nikon Eclipse Ti)、流式细胞仪(BD Biosciences)、光电血液分析仪(MEK-7222K)。
1.3 实验方法
1.3.1 GTKO五指山小型猪的繁育
由体细胞核移植技术获得GGTA1单等位基因敲除(GGTA1+/-)五指山小型猪2只(雌性、雄性各1只)和GGTA1双等位基因敲除(GGTA1-/-)五指山小型猪1只(雄性)组成F0代群体,繁育获得F1代GTKO五指山小型猪群;选育母性好、繁殖性能良好的F1代雌性个体进行繁育获得F2代猪群。
1.3.2 窝产仔数统计
记录连续2代GTKO五指山小型猪繁育情况,统计窝产仔数和断奶后仔猪存活情况,分析初产和经产雌性猪窝产仔数、断奶后仔数存活的平均值和标准差。
1.3.3 仔猪GGTA1基因敲除类型鉴定
同源重组GGTA1基因敲除类型鉴定,剪取五指山小型猪的耳朵,使用ZR Genomic DNATM-Tissue MiniPrep试剂盒提取DNA进行聚合酶链反应(PCR),然后将产物进行电泳。PCR反应条件:95 ℃预变性5 min,95 ℃变性30 s,67 ℃退火30 s,72 ℃延伸2 min,32个循环,72 ℃终延伸10 min,4 ℃保存。引物信息见表 1。
表 1 本研究中使用的引物信息Table 1. Information of primers used in the study引物名称 引物序列(5’-3’) 引物用途 产物长度 退火温度(℃) TALEN-F1/R1 F1:AGGGACAGTAGACCTAGGAAAC 鉴定TALEN敲除类型 652 bp 60 R1: GATCCTAATTGGGTTTGCTGCC Neo-F/R F:GGATGCTTCCTCTAGTCTGTGATG 鉴定同源重组敲除类型 942 bp/ 2 005 bp 67 R:CTCTAGCCTACCCAGAACTGCAGAG 利用TALEN敲除GGTA1基因的仔猪类型鉴定,提取DNA方法如上,PCR纯化回收目的片段进行TA克隆,涂板培养12 h后,每板挑取10个菌落送至北京中美泰和生物技术公司测序。MagAlign软件比对序列信息确定GGTA1基因敲除类型[6]。PCR扩增反应体系 (20 μL):上下游引物F/R(10 pmol/L)各1 μL,DNA模板(85 ng/μL)1 μL,Premix LA Taq (LA Taq) 10 μL,双蒸水(ddH2O)7 μL。PCR反应条件:95 ℃预变性5 min,95 ℃变性30 s,60 ℃退火30 s,72 ℃延伸45 s,32个循环,72 ℃终延伸10 min,4 ℃保存。引物信息见表 1。
1.3.4 αGal表型鉴定
全血裂解法分离外周血单核细胞(peripheral blood mononuclear cell,PBMC),利用FITC-BS-I-B4染色,荧光显微镜和流式细胞术检测荧光强度鉴定αGal表型,分析GGTA1基因敲除情况。吸取0.1 mL五指山小型猪全血及0.1 mL志愿者全血作为对照,加入1 mL 1×BD Pharm LyseTM裂解红细胞,常温裂解15 min,离心后去除上清,加入2 mL杜氏磷酸盐缓冲液(DPBS),离心后去除上清,重复2次;获得混合碎片的PBMC;用1~2 μL含量为1 g/L的FITC-GSIB4与PBMC冰上避光孵育30 min,加入2 mL DPBS,离心后去除上清,重复2次;500 μL DPBS重悬细胞,倒置荧光显微镜和流式细胞仪观察。
1.3.5 血常规检测
随机挑选3只成年GTKO五指山小型猪,另选3只成年野生型五指山小型猪为对照,采血前禁食16 h,清醒状态下前腔静脉采集2 mL全血,置于EDTA-K2抗凝管中。使用光电血液分析仪检测白细胞计数、红细胞计数、血红蛋白、红细胞比容、红细胞平均容积、红细胞平均血红蛋白含量、红细胞平均血红蛋白浓度、红细胞分布宽度、血小板计数、血小板比容、平均血小板容积、血小板分布宽度、淋巴细胞计数、单核细胞计数、中性粒细胞计数、淋巴细胞百分数、单核细胞百分数、中性粒细胞百分数共18项指标,参考值见文献[8]。
1.4 研究方法
统计GTKO五指山小型猪的繁育结果及窝产仔数;采用PCR技术对GTKO五指山小型猪GGTA1基因敲除类型进行鉴定;采用荧光显微镜和流式细胞术对人、野生型五指山小型猪、GTKO五指山小型猪PBMC的αGal表型进行检测;比较GTKO五指山小型猪与野生型五指山小型猪血常规指标的差异。
1.5 统计学方法
采用SPSS 21.0软件进行统计学分析。计量资料采用均数±标准差表示,多组之间比较采用方差分析。率的比较采用χ 2检验分析。P<0. 05表示差异有统计学意义。
2. 结果
2.1 GTKO五指山小型猪的繁育结果
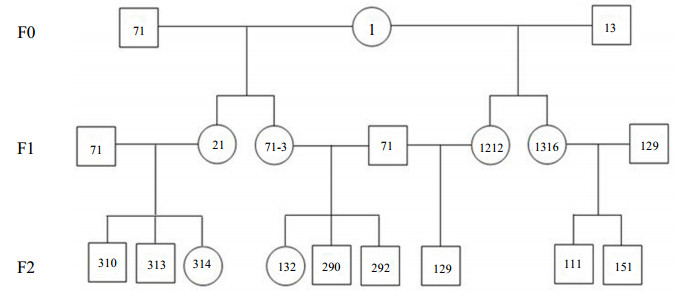
F0代雌性猪(编号1)繁育3胎共获得22只F1代GGTA1基因敲除五指山小型猪,选出4只雌性猪(编号21、71-3、1212、1316)建立F1代基础雌性猪群;F1代配种后获得F2代GGTA1基因敲除五指山小型猪56只。部分五指山小型猪系谱图(图 1)。
2.2 窝产仔数统计结果
GTKO五指山小型猪中,初产(第1胎)雌性猪窝产仔数量为(6.8±1.8)只,存活仔猪数量为(6.4±2.1)只;经产(已分娩1胎及以上)雌性猪窝产仔数量为(8.3±2.2)只,存活仔猪数量为(6.6±1.6)只(表 2)。
表 2 GTKO五指山猪产仔数量及存活仔数Table 2. Litter amount and survival of piglets of GTKO Wuzhishan miniature pigs代系 雌性猪 雄性猪 胎次(胎) 窝产仔数(只) 存活仔猪(只) F1 1(F0) 13 1 8 8 13 2 8 8 71 3 11 6 F2 71-3(F1) 71 1 4 3 71 2 10 7 71 3 10 9 1212(F1) 71 1 8 8 129 2 8 6 1316(F1) 129 1 6 6 129 2 5 4 32 3 6 6 21(F1) 71 1 8 7 2.3 GGTA1基因敲除类型鉴定结果
GGTA1+/-雌性猪与GGTA1-/-雄性猪配种3窝,共产仔23只,GGTA1-/-8只、GGTA1+/-15只;GGTA1+/-雌性猪与GGTA1+/-雄性猪配种7窝,共产仔47只,GGTA1-/-15只、GGTA1+/-20只、GGTA1+/+ 12只。GGTA1基因型能稳定遗传给后代,基本符合孟德尔遗传定律。
2.4 αGal表型检测
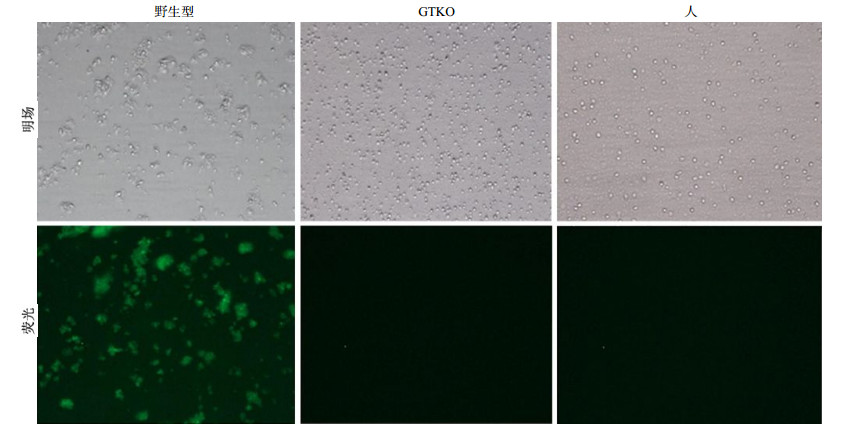
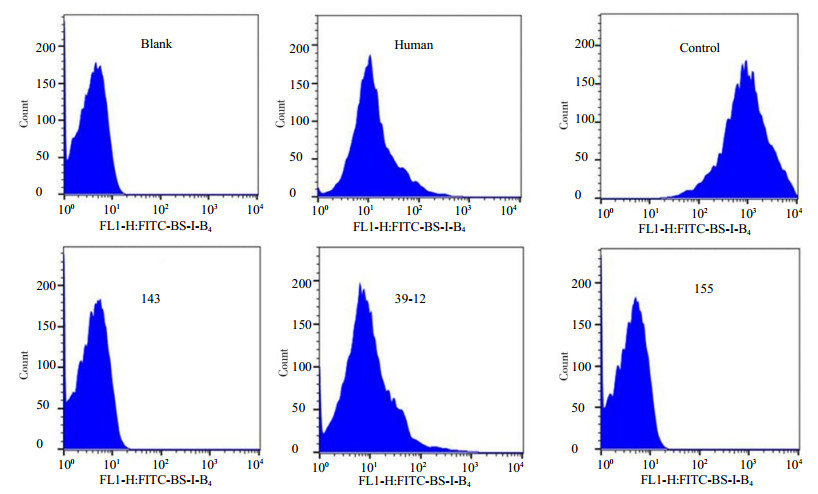
荧光显微镜和流式细胞术检测结果显示(图 2、3),野生型五指山小型猪PBMC的荧光强度高;人PBMC未检测到荧光信号;GTKO五指山小型猪PBMC的荧光强度与人PBMC的荧光强度几乎一致,表明GGTA1基因敲除,彻底去除了猪细胞表面的αGal表型。
2.5 GTKO五指山小型猪血常规检测结果
血常规结果显示(表 3),GTKO五指山小型猪与野生型五指山小型猪的各项血液生理指标比较,差异均无统计学意义(均为P>0.05),表明GGTA1基因敲除对猪的生理状况无明显影响。
表 3 GTKO与野生型五指山小型猪血液生理指标的比较Table 3. Comparison of blood routine indexes between GTKO and wild-type Wuzhishan miniature pig血液生理指标 GTKO五指山小型猪(n=3) 野生型五指山小型猪(n=3) 五指山小型猪参考值[8] 白细胞计数 (109/L) 20.8±10.0 18.4±2.1 10.2~24.6 红细胞计数 (1012/L) 9.2±1.9 8.2±1.3 6.4~9.5 血红蛋白 (g/L) 166±37 177±62 142~217 红细胞比容(%) 45.6±9.4 50.1±18.4 38.4~69.2 红细胞平均容积(FL) 49.6±2.9 47.1±5.1 54.5~73.2 红细胞平均血红蛋白含量(pg) 18.0±0.9 16.7±1.5 16.5~22.5 红细胞平均血红蛋白浓度 (109/L) 363±9 355±7 299~329 红细胞分布宽度(%) 16.4±1.5 16.0±1.3 15.6~19.3 血小板计数(109/L) 409±316 345±61 144~387 血小板比容(%) 0.33±0.24 0.27±0.03 0.12~0.29 血小板平均容积(FL) 8.0±1.1 8.1±0.8 7.3~14.1 血小板分布宽度(%) 14.7±0.5 13.9±1.1 14.3~18.2 淋巴细胞计数 (109/L) 7.3±3.9 9.9±3.7 3.5~15.7 单核细胞计数 (109/L) 2.2±1.0 1.7±0.3 0.5~2.0 中性粒细胞计数 (109/L) 7.5±2.6 6.4±1.7 1.3~8.2 淋巴细胞百分数(%) 34.9±6.2 44.8±6.2 32.8~71.5 单核细胞百分数(%) 7.0±0.3 6.6±0.1 0.2~4.5 中性粒细胞百分数(%) 48.3±11.4 32.5±15.9 19.6~63.8 3. 讨论
猪作为异种器官移植的供体,不仅需要解决超急性排斥反应,还需解决急性血管性排斥反应、细胞性排斥反应和一系列慢性排斥反应。解决这些排斥反应需要在GTKO猪的基础上进行敲除抗原或人源化基因修饰[9-11],并转入人的补体调控因子、血栓调节蛋白等基因[12-14]。因此,GTKO猪的繁育非常重要。
本研究发现GGTA1基因敲除没有影响猪的繁殖和健康。连续2代GGTA1基因敲除五指山小型猪繁育正常,窝产仔数符合普通五指山小型猪初产雌性猪窝产仔4~6只,经产雌性猪窝产仔6~8只的生产规律[15]。F0代GGTA1+/-雌性(编号1)6岁时配种正常妊娠。子代GGTA1-/-雄性猪、GGTA1+/-雄性猪和GGTA1+/-雌性猪均能正常繁育,但获得的部分GGTA1-/-雌性猪不能正常繁育,可能的原因是GGTA1基因纯合敲除影响雌性猪的繁育,关于GGTA1基因纯合敲除如何对雌性猪繁殖产生影响有待进一步观察。GGTA1基因型遗传稳定,基本符合孟德尔遗传定律。杂合子雌性猪与纯合子雄性猪繁育的后代纯合子与杂合子的比例为8︰15,偏离孟德尔遗传学的分离定律1︰1的比例,主要原因是繁殖样本较少。血常规检测表明GTKO五指山小型猪生理健康良好。
窦科峰等[16]采用GGTA1-/-五指山小型猪为供体,藏酋猴为受体完成异种肝移植实验,受体和移植肝存活2周,无超急性排斥反应,间接表明了本实验室培育的GTKO五指山小型猪去除了细胞表面的αGal表型。猪-猴异种肝移植研究的肝供体最好为1~2月龄仔猪,在移植时肝脏大小比较合适。移植前猪αGal表型鉴定,常规方法是分离血液中PBMC,至少需要1~2 mL全血,仔猪前腔采血容易损伤脏器产生应激反应。全血裂解分离PBMC,仅需0.1 mL全血,从而减小对供体的伤害。
总之,本研究系统研究了GGTA1基因敲除五指山小型猪的繁育和鉴定,连续2代跟踪研究表明遗传稳定、繁殖正常,并建立了GTKO五指山小型猪家系及微量血液检测αGal表型的方法。
-
表 1 本研究中使用的引物信息
Table 1 Information of primers used in the study
引物名称 引物序列(5’-3’) 引物用途 产物长度 退火温度(℃) TALEN-F1/R1 F1:AGGGACAGTAGACCTAGGAAAC 鉴定TALEN敲除类型 652 bp 60 R1: GATCCTAATTGGGTTTGCTGCC Neo-F/R F:GGATGCTTCCTCTAGTCTGTGATG 鉴定同源重组敲除类型 942 bp/ 2 005 bp 67 R:CTCTAGCCTACCCAGAACTGCAGAG 表 2 GTKO五指山猪产仔数量及存活仔数
Table 2 Litter amount and survival of piglets of GTKO Wuzhishan miniature pigs
代系 雌性猪 雄性猪 胎次(胎) 窝产仔数(只) 存活仔猪(只) F1 1(F0) 13 1 8 8 13 2 8 8 71 3 11 6 F2 71-3(F1) 71 1 4 3 71 2 10 7 71 3 10 9 1212(F1) 71 1 8 8 129 2 8 6 1316(F1) 129 1 6 6 129 2 5 4 32 3 6 6 21(F1) 71 1 8 7 表 3 GTKO与野生型五指山小型猪血液生理指标的比较
Table 3 Comparison of blood routine indexes between GTKO and wild-type Wuzhishan miniature pig
血液生理指标 GTKO五指山小型猪(n=3) 野生型五指山小型猪(n=3) 五指山小型猪参考值[8] 白细胞计数 (109/L) 20.8±10.0 18.4±2.1 10.2~24.6 红细胞计数 (1012/L) 9.2±1.9 8.2±1.3 6.4~9.5 血红蛋白 (g/L) 166±37 177±62 142~217 红细胞比容(%) 45.6±9.4 50.1±18.4 38.4~69.2 红细胞平均容积(FL) 49.6±2.9 47.1±5.1 54.5~73.2 红细胞平均血红蛋白含量(pg) 18.0±0.9 16.7±1.5 16.5~22.5 红细胞平均血红蛋白浓度 (109/L) 363±9 355±7 299~329 红细胞分布宽度(%) 16.4±1.5 16.0±1.3 15.6~19.3 血小板计数(109/L) 409±316 345±61 144~387 血小板比容(%) 0.33±0.24 0.27±0.03 0.12~0.29 血小板平均容积(FL) 8.0±1.1 8.1±0.8 7.3~14.1 血小板分布宽度(%) 14.7±0.5 13.9±1.1 14.3~18.2 淋巴细胞计数 (109/L) 7.3±3.9 9.9±3.7 3.5~15.7 单核细胞计数 (109/L) 2.2±1.0 1.7±0.3 0.5~2.0 中性粒细胞计数 (109/L) 7.5±2.6 6.4±1.7 1.3~8.2 淋巴细胞百分数(%) 34.9±6.2 44.8±6.2 32.8~71.5 单核细胞百分数(%) 7.0±0.3 6.6±0.1 0.2~4.5 中性粒细胞百分数(%) 48.3±11.4 32.5±15.9 19.6~63.8 -
[1] Meurens F, Summerfield A, Nauwynck H, et al. The pig: a model for human infectious diseases[J]. Trends Microbiol, 2012, 20(1): 50-57. DOI: 10.1016/j.tim.2011.11.002.
[2] Tuggle CK, Green JA, Fitzsimmons C, et al. EST-based gene discovery in pig: virtual expression patterns and comparative mapping to human[J]. Mamm Genome, 2003, 14(8): 565-579. DOI: 10.1007/s00335-002-2263-7
[3] Denning C, Burl S, Ainslie A, et al. Deletion of the α (1, 3) galactosyl transferase (GGTA1) gene and the prion protein (PrP) gene in sheep[J]. Nat Biotechnol, 2001, 19(6): 559-562. DOI: 10.1038/89313
[4] Lai L, Kolber-Simonds D, Park KW, et al. Production of α-1, 3-galactosyltransferase knockout pigs by nuclear transfer cloning[J]. Science, 2002, 295(5557): 1089-1092. DOI: 10.1126/science.1068228
[5] 郑道山, 冯冲, 朱彦宾, 等.利用启动子缺陷型打靶载体敲除五指山小型猪GGTA1基因[J].生物技术通讯, 2011, 22(4): 458-462. DOI: 10.3969/j.issn.1009-0002.2011.04.002. Zheng DS, Feng C, Zhu YB, et al. Knockout of GGTA1 Gene by Promoter-Trap Strategy in Wuzhishan Miniature Pig[J]. Lett Biotechnol, 2011, 22(4): 458-462. DOI: 10.3969/j.issn.1009-0002.2011.04.002.
[6] Feng C, Li XR, Cui HT, et al. Highly efifcient generation of GGTA1 knockout pigs using a combination of TALEN mRNA and magnetic beads with somatic cell nuclear transfer[J]. J Integr Agr, 2016, 15(7): 1540-1549. DOI: 10.1016/S2095-3119(16)61347-3
[7] Nottle MB, Beebe LF, Harrison SJ, et al. Production of homozygous alpha-1, 3-galactosyltransferase knockout pigs by breeding and somatic cell nuclear transfer[J]. Xenotransplantation, 2007, 14(4): 339-344. DOI: 10.1111/xen.2007.14.issue-4
[8] 杨述林, 任红艳, 王恒, 等.中国实验用小型猪种群血液生理指标分析[J].中国畜牧兽医, 2007, 34(2): 38-41. DOI: 10.3969/j.issn.1671-7236.2007.02.013. Yang SL, Ren HY, Wang H, et al. Investigation on the hematology parameters of Chinese laboratory miniature pig breeds[J]. Chin Anim Husb Vet Med, 2007, 34(2): 38-41. DOI: 10.3969/j.issn.1671-7236.2007.02.013.
[9] 曾国敏, 蒋应弟, 冯冲, 等.表达人CD47基因的巴马小型猪创建及其表达分析[J].农业生物技术学报, 2016, 24(8): 1251-1258. DOI: 10.3969/j.issn.1674-7968.2016.08.017. Zeng GM, Jiang YD, Feng C, et al. Generation and expression analysis of human (homo sapiens) CD47 transgenic bama miniature pig (sus scrofa)[J]. J Agric Biotechnol, 2016, 24(8): 1251-1258. DOI: 10.3969/j.issn.1674-7968.2016.08.017.
[10] Burlak C, Bern M, Brito AE, et al. N-linked glycan profiling of GGTA1/CMAH knockout pigs identifies new potential carbohydrate xenoantigens[J]. Xenotransplantation, 2013, 20(5): 277-291. DOI: 10.1111/xen.12047.
[11] Estrada JL, Martens G, Li P, et al. Evaluation of human and non-human primate antibody binding to pig cells lacking GGTA1/CMAH/β4GalNT2 genes[J]. Xenotransplantation, 2015, 22(3): 194-202. DOI: 10.1111/xen.12161.
[12] Van Der Windt DJ, Bottino R, Casu A, et al. Long-term controlled normoglycemia in diabetic non-human primates after transplantation with hCD46 transgenic porcine islets[J]. Am J Transplant, 2009, 9(12): 2716-2726. DOI: 10.1111/j.1600-6143.2009.02850.x.
[13] Sun X, Funk CD, Deng C, et al. Role of decay-accelerating factor in regulating complement activation on the erythrocyte surface as revealed by gene targeting[J]. Proc Natl Acad Sci U S A, 1999, 96(2): 628-633. DOI: 10.1073/pnas.96.2.628
[14] Esmon CT. The protein C pathway[J]. Chest, 2003, 124(3 suppl): 26S-32S.
[15] 闵凡贵, 潘金春, 袁文, 等.五指山小型猪繁殖性能测定[J].实验动物与比较医学, 2011, 31(5): 349-351. DOI: 10.3969/j.issn.1674-5817.2011.05.009. Min FG, Pan JC, Yuan W, et al. Determination of reproductive performance of outbred wuzhishan minipigs[J]. Lab Anim Comp Med, 2011, 31(5): 349-351. DOI: 10.3969/j.issn.1674-5817.2011.05.009.
[16] 窦科峰, 李霄, 陶开山, 等.异种肝移植现状与未来[J].中国实用外科杂志, 2014, 34(1): 14-18. http://www.cnki.com.cn/Article/CJFDTOTAL-ZGWK201401007.htm Dou KF, Li X, Tao KS, et al. The status quo and future of xenotransplantation[J]. Chin J Pract Surg, 2014, 34(1): 14-18. http://www.cnki.com.cn/Article/CJFDTOTAL-ZGWK201401007.htm
-
期刊类型引用(3)
1. 陈雨荣,安星兰,张胜,翟岩辉,于浩,代相鹏,李子义. 中国小型猪在生物医药领域的研究进展. 中国实验动物学报. 2021(05): 695-706 .  百度学术
百度学术
2. 杜敏杰,魏静,臧荣鑫,潘登科. 流式细胞术检测供体猪α-1, 3-Gal和人源CD46的表达. 实用器官移植电子杂志. 2018(05): 375-379 .  百度学术
百度学术
3. 杨佩军,李霄,窦科峰. GTKO猪α-1, 3-半乳糖苷转移酶检测方法的进展. 实用器官移植电子杂志. 2018(05): 409-411 .  百度学术
百度学术
其他类型引用(1)



 下载:
下载: